- Transfer teknologi untuk vaksin DPT-HepB-Hib (Pentavalen) bersama Netherlands Vaccine Institute pada tahun 2004.
- Kepemimpinan di tingkat global, termasuk saat Bio Farma dipercaya menjadi Chair of the Board DCVMN periode 2023-2025, yang menjadikan Indonesia sebagai jembatan antara anggota jejaring dan arah strategis global.
- Komitmen Bio Farma terhadap inovasi telah menempatkan Indonesia di garis depan kemajuan teknologi vaksin di negara berkembang. Melalui kolaborasi, riset, dan transfer pengetahuan, Bio Farma tidak hanya memperkuat kemandirian nasional di bidang kesehatan, tetapi juga menjadi katalisator peningkatan kapasitas produksi vaksin global.
Merekam Jejak Indonesia di DCVMN dan Keberhasilan Soal Vaksin

Indonesia dipercaya DCVMN beberapa kali, menunjukkan kontribusi nyata dan teknis Bio Farma dalam jejaring global.
Bio Farma berkontribusi melalui transfer teknologi vaksin, kepemimpinan global, dan komitmen terhadap inovasi di industri vaksin.
Bio Farma mencapai sejarah dunia dengan keberhasilan vaksin polio nOPV2, membentuk fondasi regulasi EUL yang dijadikan acuan WHO saat pandemi COVID-19.
Denpasar, IDN Times - Perjalanan Indonesia bersama Developing Countries Vaccine Manufacture Network (DCVMN) telah berlangsung lebih dari dua dekade. Sejak didirikan di Noordwijk pada tahun 2000, Bio Farma menjadi salah satu dari 10 anggota pendiri yang membentuk dasar kolaborasi global antarnegara berkembang di bidang vaksin.
President Director PT Bio Farma, Shadiq Akasya, menjelaskan bahwa setahun kemudian, pada 2001, Bandung dipercaya menjadi tuan rumah AGM ke-2 DCVMN, di mana struktur kelembagaan dan tata kelola jaringan pertama kali disepakati.
"Itu adalah tonggak sejarah yang menempatkan Indonesia sebagai salah satu hub kolaborasi dan pengetahuan bagi produsen vaksin dunia," tuturnya.
1. Beberapa kali Indonesia dipercaya DCVMN
Menurut Shadiq, pada tahun 2004, Bio Farma bersama anggota DCVMN lainnya berperan penting dalam meningkatkan akses terhadap vaksin kombinasi DPT-HepB-Hib, hasil kolaborasi transfer teknologi dengan Netherlands Vaccine Institute. Keberhasilan ini menunjukkan bahwa kontribusi Bio Farma dalam jejaring DCVMN bersifat nyata dan teknis, bukan sekadar simbolis.
Selanjutnya, pada 2012, Indonesia kembali dipercaya menjadi tuan rumah AGM ke-13 DCVMN di Bali, di mana Mahendra Suhardono, salah satu Direksi Bio Farma saat itu, terpilih sebagai Presiden Executive Committee Member DCVMN periode 2013–2014.
“Setelah 13 tahun, Indonesia kembali dipercaya menyelenggarakan pertemuan ke-26, menandai kontinuitas kepemimpinan dan kredibilitas Indonesia di mata dunia,” ungkapnya.
Kepemimpinan Indonesia di DCVMN semakin diakui ketika Bio Farma, yang diwakili oleh Adriansjah Azhari, dipercaya menjabat sebagai Chair of The Board DCVMN periode 2023–2025. Posisi ini menegaskan peran Bio Farma sebagai jembatan antara anggota jejaring dan arah strategis global, sekaligus simbol kapasitas Indonesia dalam memimpin industri vaksin negara berkembang.
2. Tiga langkah kontribusi Indonesia dalam industri vaksin
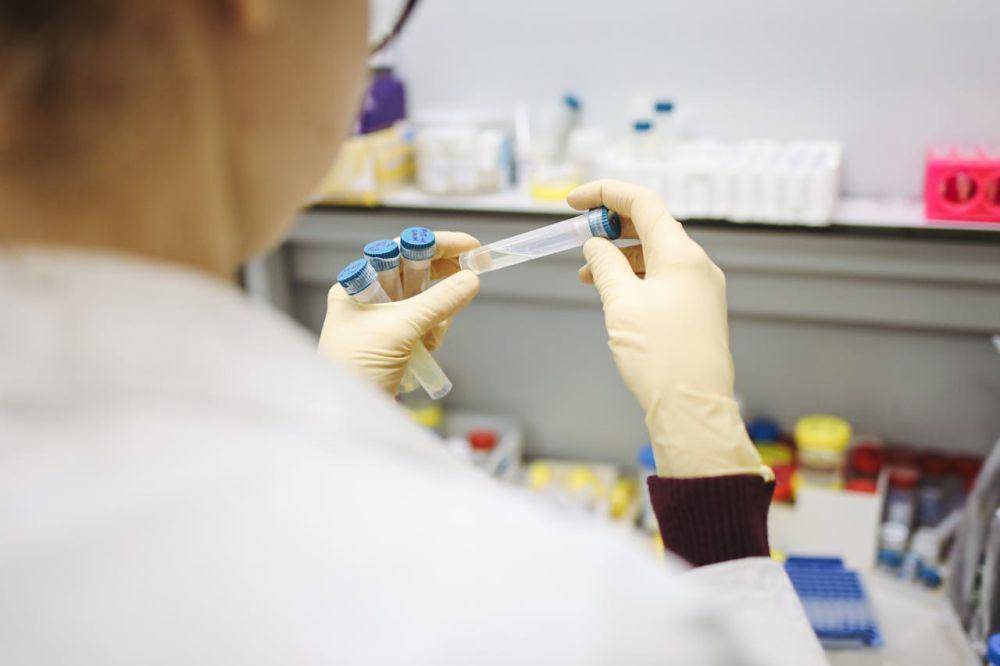
Lebih lanjut, peran Bio Farma di DCVMN diungkapnya bukan sekadar simbol representasi nasional. Ini adalah bentuk kontribusi nyata Indonesia bagi ketahanan kesehatan global. Melalui berbagai inisiatif kolaboratif, Bio Farma telah berkontribusi di antaranya:
3. Bio Farma menorehkan sejarah dunia melalui vaksin polio
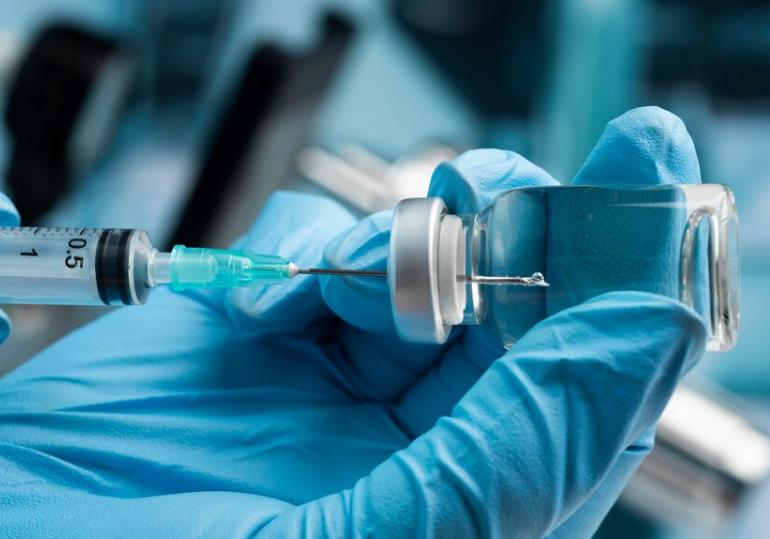
Shadiq melanjutkan bahwa komitmen terhadap inovasi tersebut mencapai puncaknya pada tahun 2020. Bio Farma menorehkan sejarah dunia melalui keberhasilan vaksin novel Oral Polio Vaccine type 2 (nOPV2), yang menjadi vaksin pertama di dunia yang memperoleh status Emergency Use Listing (EUL) dari WHO.
"Pencapaian ini bukanlah proses yang mudah, karena menjadi yang pertama di dunia. WHO saat itu belum memiliki standar maupun regulasi yang mapan untuk prosedur EUL. Hal ini menjadikan perjalanan Bio Farma penuh tantangan, sebab banyak dokumen dan persyaratan baru yang harus dikembangkan dan disesuaikan secara dinamis bersama WHO," jelasnya.
Dalam proses tersebut, Bio Farma bekerja intensif bersama Badan Pengawas Obat dan Makanan (BPOM), serta mitra pengembangan seperti Gates Foundation dan PATH, untuk memastikan seluruh proses pemenuhan persyaratan EUL berjalan sesuai prinsip keamanan, mutu, dan efikasi. Kolaborasi ini bukan hanya menghasilkan izin penggunaan darurat pertama di dunia, tetapi juga membentuk fondasi regulasi EUL yang kemudian dijadikan acuan WHO saat menghadapi pandemi COVID-19.
"Dengan kata lain, pengalaman dan pelajaran dari nOPV2 menjadi dasar terbentuknya standar global yang lebih siap digunakan dalam situasi darurat kesehatan berikutnya. Inovasi ini bukan hanya pencapaian teknis, tapi juga simbol kemandirian teknologi dan kepercayaan dunia terhadap kapasitas Indonesia," pungkasnya.